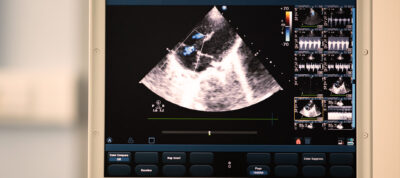
Manutenção da anticoagulação após a angioplastia primária no IAM com supradesnivelamento do segmento ST: estudo RIGHT
Escrito por: Flávia Bittar Brito Arantes em 4 de abril de 2024
5 min de leitura
Referências
Yan Y, Guo J, Wang X, et al; on behalf of RIGHT Investigators. Postprocedural Anticoagulation After Primary Percutaneous Coronary Intervention for ST-Segment-Elevation Myocardial Infarction: A Multicenter, Randomized, Double-Blind Trial. Circulation. 2024 Feb 26. doi: 10.1161/CIRCULATIONAHA.123.067079. Epub ahead of print. PMID: 38406848.
Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, Claeys MJ, Dan GA, Dweck MR, Galbraith M, et al; ESC Scientific Document Group. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J. 2023;44:3720–3826.
O’Gara PT, Kushner FG, Ascheim DD, Casey DE Jr, Chung MK, de Lemos JA, Ettinger SM, Fang JC, Fesmire FM, Franklin BA, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2013;61:e78–e140.
Serrano Junior CV, Fenelon G, Soeiro AM, Nicolau JC, Piegas LS, Montenegro ST, et al. Sociedade Brasileira de Cardiologia. Diretrizes Brasileiras de Antiagregantes Plaquetários e Anticoagulantes em Cardiologia. Arq Bras Cardiol 2013; 101 (3Supl.3): 1-93
Flávia Bittar Brito Arantes
Professora Adjunta da Faculdade de Medicina da Universidade Federal de Uberlândia, Docente na Faculdade IMEPAC, Coordenadora Médica do Centro de Pesquisa Eurolatino em Uberlândia e Ex-aluna da pós-graduação de pesquisa clínica Med.IQ.

 Vea MedIQ en Español
Vea MedIQ en Español